71
Нарисуйте энергетическую схему образования молекулы He2 и молекулярного иона He2+ по методу молекулярных орбиталей. Как метод МО объясняет устойчивость иона He2+ и невозможность существования молекулы He2?
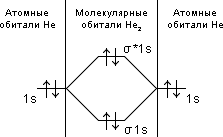
Порядок связи равен нулю, значит молекула He2 должна быть энергетически неустойчивой, поскольку здесь из четырёх электронов, которые должны разместиться на МО, два займут связывающую (1s), а два – разрыхляющую (*1s) МО. Следовательно, образование молекулы He2 не будет сопровождаться выделением энергии.

В ионе He2+ порядок связи равен 0,5, следовательно, образование данного иона будет сопровождаться выделением энергии. При его образовании два электрона занимают связывающую МО, а третий электрон – занимает разрыхляющую МО, что и приводит данную частицу к устойчивому существованию.