Задание 6
Составьте конспект ответа, характеризующего метан и этан. Оформите свой ответ в виде таблицы.
| Общая характеристика вещества | Метан | Этан |
|---|---|---|
| Молекулярная формула | CH4 | C2H6 |
| Структурная формула | 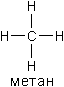 |
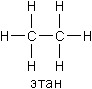 |
| Образование связей | В молекуле метана и этана атомы углерода находятся в sp3-гибридном состоянии. В молекуле метана имеются четыре C–H связи, а в молекуле этана их 6, каждая из этих связей образуется таким образом, что sp3-орбиталь атома углерода перекрывается с s-орбиталью атома водорода. |
|
В молекуле этана имеется C–C связь, которая образуется таким образом, что sp3-орбиталь одного атома углерода перекрывается с одной sp3-орбиталью другого атома углерода. |
||
Все связи относятся к σ-связям, так как они образуются в результате перекрывания орбиталей вдоль линии, соединяющих центры ядер. |
||
| Нахождение в природе | В виде залежей природного газа, в составе попутных нефтяных газов, в каменноугольных пластах, внутри ледяных кристаллов в толще вечной мерзлоты. | В составе природного газа. |
| Получение | В лаборатории получают при сплавлении ацетата натрия с гидроксидом натрия: CH3COOH + NaOH ⟶ CH4 + Na2CO3 В промышленности получают из природного газа. |
В лаборатории из иодметана с металлическим натрием: 2CH3I + 2Na ⟶ C2H6 + 2NaI В промышленности получают из природного газа. |
| Физические свойства | Бесцветный газ, без запаха и вкуса, tкип. = -161,58°C. | Бесцветный газ, без запаха и вкуса, tкип. = -88,6°C. |
| Химические свойства |
Реагирует с галогенами: Сгорает в кислороде и кислороде воздуха: Реакция дегидрирования: |
Реагирует с галогенами: Сгорает в кислороде и кислороде воздуха: Реакция дегидрирования: |
| Применение | В качестве топлива, для получения водорода и синтеза других органических соединений. | Для получения этилена. |