Задание 1
Составьте электронные формулы метилового спирта, этилового спирта и воды. Поясните, как при перекрывании соответствующих электронных орбиталей образуются химические связи в молекуле воды и в гидроксильной группе спиртов.
Электронные формулы:
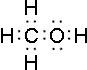
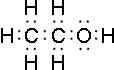
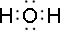
| +8O | ↑↓ | ↑↓ | ↑↓ | ↑ | ↑ | |||
| 1s | 2s | 2p | ||||||
Два неспаренных электрона атома кислорода образуют две взаимно перпендикулярные электронные орбитали гантелеобразной формы.
В молекуле воды одна 2p-орбиталь атома кислорода перекрывается c 1s-орбиталью атома водорода, вторая 2p-орбиталь также перекрывается c 1s-орбиталью другого атома водорода.
В гидроксильной группе спиртов одна 2p-орбиталь атома кислорода перекрывается c одной sp3-орбиталью атома углерода, другая 2p-орбиталь атома кислорода, которая расположена перпендикулярно первой, перекрывается c s-орбиталью атома водорода.
В молекулах этилового спирта угол между валентными электронными орбиталями атома кислорода равен 110°, примерно такой же угол имеется и в молекулах других одноатомных спиртов. В молекуле воды он немного меньше – около 105°.