Задание 2
Почему численное значение валентности не всегда совпадает с числом электронов на наружном энергетическом уровне?
Численное значение валентности не всегда совпадает с числом электронов на наружном энергетическом уровне, это связано с тем, что в образовании связей участвуют неспаренные электроны.
Например, у атома серы на внешнем энергетическом уровне находится 6 электронов. В нормальном состоянии у серы только два электрона являются неспаренными:
| 16S | ↑↓ | ↑↓ | ↑ | ↑ | ||||||||
| 3s | 3p | 3d | ||||||||||
Действительно, известны соединения двухвалентной серы, например сероводород H2S.
У атома серы на наружном энергетическом уровне имеются свободные d-орбитали, то в результате распаривания 3p- и 3s-электронов может образоваться четыре или шесть неспаренных электронов:
| 16S | ↑↓ | ↑ | ↑ | ↑ | ↑ | |||||||
| 3s | 3p | 3d | ||||||||||
| 16S | ↑ | ↑ | ↑ | ↑ | ↑ | ↑ | ||||||
| 3s | 3p | 3d | ||||||||||
Отсюда вытекает то, что сера может быть четырёхвалентна, например в оксиде серы (IV) SO2, и шестивалентна, например в оксиде серы (VI) SO3.
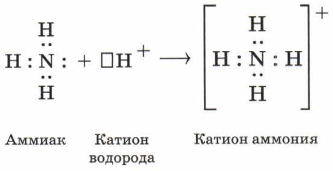
Однако валентные возможности атомов определяются не только числом неспаренных электронов, но и числом неподелённых электронных пар, способных переходить на свободные орбитали атомов другого элемента. Это подтверждается процессом образования ионов аммония и гидроксония.